
电化学电池是一种可以从其中发生的化学反应中产生电能或使用提供给它的电能来促进其中的化学反应的装置。这些设备能够将化学能转化为电能,反之亦然。电化学电池的一个常见示例是标准的 1.5 伏电池,用于为许多电器(如电视遥控器和时钟)供电。
这种能够从其中发生的化学反应中产生电流的电池称为原电池或伏打电池。或者,当电流通过它们时引起化学反应的电池称为电解电池。
下面提供了详细说明电化学电池不同部分的图表。
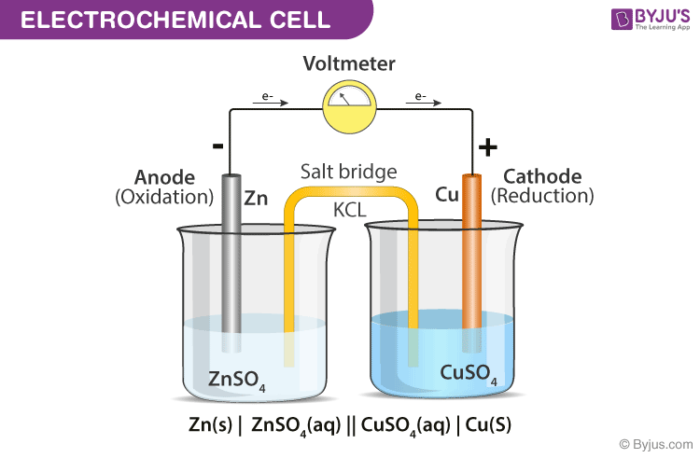
电化学电池
电化学电池通常由阴极和阳极组成。阴极和阳极的主要特征如下表所示。
| 阴极 | 阳极 |
| 用正号表示,因为这里消耗了电子 | 用负号表示,因为电子在这里被释放 |
| 还原反应发生在电化学电池的阴极 | 此处发生氧化反应 |
| 电子进入阴极 | 电子离开阳极 |
一般约定规定阴极必须表示在右侧,而阳极表示在左侧,同时表示电化学电池。
两种主要类型的电化学电池是
1.原电池(也称为伏打电池)
2. 电解槽
原电池和电解电池之间的主要区别如下表所示。
| 原电池/伏打电池 | 电解槽 |
| 在这些电化学电池中,化学能转化为电能。 | 电能在这些细胞中转化为化学能。 |
| 在这些细胞中发生的氧化还原反应本质上是自发的。 | 在这些电池中进行氧化还原反应需要输入能量,即反应是非自发的。 |
| 在这些电化学电池中,阳极带负电,阴极带正电。 | 这些电池具有带正电的阳极和带负电的阴极。 |
| 电子来源于经历氧化的物质。 | 电子来自外部来源(例如电池)。 |
盐桥完成了电化学电池的电路,从而允许电流通过它。它还有助于保持电池的整体电中性。
电极的标准电极电位可以定义为在标准条件(温度 = 298K,压力 = 1 个大气压,反应物质的统一浓度)下电极和电解质之间产生的电位差。它由符号“E o cell ”表示。单击此处了解有关标准电极电位的更多信息。
电化学电池的阴极是发生还原的位置。它通常用正 (+) 号表示。电子从阳极流向阴极。在电化学电池中,阳极是发生氧化的电极。它用负号 (-) 表示。
是的,电解池的阳极带正电(阴极带负电)。然而,尽管有负电荷,但阳极仍会发生氧化。在这些电化学电池中发生的化学反应本质上是非自发的。
电解电池是一类使用电流来促进电池反应的电化学电池。这种细胞内部发生的化学反应通常被称为电解。电解池可用于将铝土矿分解成铝和其他成分。这种电池也可用于将水电解成氢气和氧气。
因此,讨论了电化学电池的关键概念和类型。要了解有关电化学相关重要概念的更多信息,例如能斯特方程,请在 BYJU'S 注册并在智能手机上下载移动应用程序。